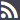Primeros resultados de estudios preclínicos de vacunas frente a SARS-CoV-2
Autores:
Lucía García San Miguel.
Centro de Coordinación de Alertas y Emergencias Sanitarias, Ministerio de Sanidad.
Agustín Portela Moreira.
Jefe del Servicio de Biotecnología, Departamento de Medicamentos de Uso Humano de la AEMPS.
El 6 de mayo de 2020 se han publicado en la revista Science los resultados de la investigación preclínica, así como algunos detalles, de la fabricación de la vacuna PiCoVacc, de la compañía Sinovac Biotech Ltd., de Pekín, China (Q. Gao et al, Science: 10.1126/science.abc1932 (2020)). La novedad de esta publicación es que es la primera que describe la immunogenicidad (incluyendo anticuerpos neutralizantes) de una vacuna frente a SARS-CoV-2 en modelos animales y la protección en un modelo de primates, y hacen pensar que se va a disponer de vacunas eficaces frente a la enfermedad causada por el virus SARS-CoV-2 en humanos. El 14 de mayo, “ahead of print” hay otra publicación con resultados muy favorables de seguridad y eficacia en modelos animales de una segunda vacuna, la ChAdOx1 nCoV-19 de Vaccitech.
Si bien hay otras compañías que trabajan en vacunas frente a COVID-19 que tienen datos similares a los descritos en esta publicación, no están en el domino público.
En resumen, los datos de protección en modelos animales con estas dos vacunas indican claramente que el desarrollo de una vacuna eficaz y segura para humanos es posible, si bien aún queda un largo camino por recorrer para disponer de ella.
Desarrollo rápido de una vacuna inactivada candidata para el SARS-CoV-2(1).
El principio activo de PiCoVacc son viriones completos de SARS-CoV-2 crecidos en cultivos de células Vero, inactivados con β-propiolactona (que es un agente utilizado en la inactivación de vacunas inactivadas de gripe) y adyuvada con hidróxido de aluminio. Tras crecer en células, el virus se inactiva y se purifica exhaustivamente.
La experimentación preclínica se llevó a cabo en ratones, ratas y macacos, en los que se probaron distintas dosis de antígeno y de adyuvante. En ratones inmunizados con dos dosis (día 0 y día 7) se demostró que la vacuna es capaz de inducir una respuesta inmune específica (parte superior de la figura 1) medida por ELISA y con capacidad de generar anticuerpos neutralizantes (parte inferior de la figura 1). Los anticuerpos generados en los roedores estaban en su mayoría dirigidos a la proteína S (spike) completa o a su dominio de unión al receptor (RBD) y en menor medida a la proteína N del virus. Se compararon además los anticuerpos obtenidos en ratones vacunados (parte A de la figura 1) con los de pacientes humanos que han pasado COVID-19 (parte B de la figura 1). Los títulos de anticuerpos medidos por ELISA y los neutralizantes obtenidos en ratones vacunados fueron muy superiores a los detectados en pacientes recuperados de la infección por SARS-CoV-2. Si esto se mantuviera en humanos vacunados sería una indicación de que la vacuna sería eficaz.
Figura 1. La inmunización con PiCoVacc induce en ratones una respuesta de anticuerpos neutralizantes.
S: proteína S (spike); RBD: proteína de unión al receptor; N: proteína N; Sham: adyuvante; RECOV: sueros de personas recuperadas de COVID-19; NI: sueros de personas no infectadas por SARS-CoV-2. Arriba: respuestas específicas de IgG medidas por ELISA en ratones (A) y humanos (B); Abajo: anticuerpos neutralizantes determinados por ensayos de neutralización en ratones (A) y humanos (B).
Para estudiar la eficacia protectora de la vacuna se utilizaron macacos como modelo animal de la enfermedad COVID-19 humana. Los macacos sufren síntomas muy similares a los humanos aunque no llegan a producirse muertes por enfermedad grave. Para el ensayo de protección, se vacunaron macacos con una pauta de 3 dosis (0, 7 y 14 días), y se les administró o bien una dosis alta de vacuna adyuvada (6 µg), una dosis baja de vacuna adyuvada (3 µg), el adyuvante sin antígeno (sham) o placebo (solución salina). Una semana tras la última vacunación, se inoculó a todos los macacos con una dosis alta de virus SARS-CoV-2 por vía intratraqueal. Tras la inoculación, se demostró que los macacos vacunados con la dosis alta no presentaban manifestaciones clínicas de la enfermedad y el virus no se detectó en los órganos analizados (garganta, muestra anal y pulmón) (con la excepción de una baja carga viral en garganta en los primeros días tras la inoculación) (figura 2). Los vacunados con dosis media de la vacuna presentaron algunos síntomas y se pudo detectar virus en algunos de sus órganos, mientras que los macacos vacunados con el adyuvante (sham) y con la solución salina (placebo) tuvieron cargas virales altas en todos los órganos analizados y presentaron neumonía intersticial severa. La detección de material genético del virus en la región anal está descrita en pacientes de COVID-19, a pesar de que la transmisión no ocurre por esta vía. El hecho de no detectarse RNA viral en esta región de los animales vacunados y sí en los del grupo control da una idea de la menor replicación en general del virus en los animales vacunados.
Figura 2. Eficacia protectora de PiCoVacc en primates no humanos.
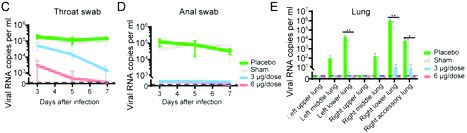
Carga viral en garganta (C), ano (D) y en varios tejidos pulmonares (E) de muestras recolectadas en los días 3, 5 y 7 tras la inoculación intrataqueal de virus SARS-CoV-2 en macacos inmunizados (con dosis de antígeno de 3 o 6 microgramos) y no inmunizados (administración de adyuvante sham o placebo).
Si bien el número de monos analizado fue pequeño, no se observó ERD (enhanced respiratory disease) ni ADE (antibody-dependent enhancement), que son agravamientos de la enfermedad observados en ensayos de inoculación de virus en animales vacunados con las vacunas desarrolladas frente a SARS y MERS. No obstante, la información aportada en la publicación es limitada y será la experimentación en humanos la que descarte completamente la posible aparición de estos fenómenos. Estos datos abren la vía a la experimentación en humanos (Fase I).
La aproximación utilizada en el desarrollo de esta vacuna es la misma que tenían las primeras vacunas de gripe de virus completo inactivado, que con el tiempo han evolucionado a vacunas de antígenos purificados ya que tienen una menor reactogenicidad que las de viriones completos.
La vacuna ChAdOx1 nCoV-19 previene la neumonía por SARS-CoV-2 en macacos rhesus.
También, muy recientemente en un artículo en prepublicación se describen los resultados de experimentación en animales con la vacuna ChAdOx1 nCoV-19, basada en un vector adenoviral de chimpancé no replicativo que expresa la proteína S del SARS-CoV-2. Esta vacuna también induce una respuesta inmune específica en ratones y en macacos, tanto a nivel de anticuerpos neutralizantes como a nivel de respuesta celular. Además, se realizaron experimentos en macacos inmunizados con una única dosis de esta vacuna, y a los que 28 días después se les inoculó virus SARS-CoV-2. Se observó que, en contraste con los animales infectados con un placebo, en los vacunados se evitaba el daño pulmonar tras la exposición y se reducía significativamente la carga y la replicación viral en el tracto respiratorio inferior. Es llamativo que, sin embargo, no hubo una reducción en la carga y replicación viral en el tracto respiratorio superior. Como se indica en la publicación ya se han iniciado ensayos de Fase 1 en humanos con la vacuna ChAdOx1 nCoV-19, en los que ya se han reclutado más de 1.000 voluntarios.
BIBLIOGRAFÍA:
- Science. Qian Gao et al. Rapid development of an inactivated vaccine candidate for SARS-CoV-2. 6.05.2020. Disponible en: https://science.sciencemag.org/content/early/2020/05/06/science.abc1932.
- bioRxiv. Neeltje van Doremalen et al. ChAdOx1 nCoV-19 vaccination prevents SARS-CoV-2 pneumonia in rhesus macaques. 13.05.2020.
(aviso: este artículo es ahead of print; no ha sido revisado por pares y desde la plataforma donde está publicado se recomienda no tomar decisiones clínicas basadas en estos resultados)
Disponible en:https://www.biorxiv.org/content/10.1101/2020.05.13.093195v1.full.pdf
 .
.
Si desea localizar información relacionada con el contenido de esta página, utilice el buscador